le Immunoélectrophorèse est utilisé pour la détection diagnostique en laboratoire des anticorps monoclonaux dans le sang d'un patient. Les anticorps monoclonaux sont dérivés de la même cellule et sont dirigés contre les mêmes antigènes. Pour cette raison, ils doivent être considérés comme pathologiques et, s'ils sont prouvés, parler de maladies telles que la maladie de Waldenström.
Qu'est-ce que l'immunoélectrophorèse?

Les ions ont une mobilité différente. Cette mobilité différente constitue la base de la procédure d'électrophérèse. Ces méthodes séparent différentes substances les unes des autres en utilisant des champs électriques et la gravité. Une méthode bien connue dans le domaine est l'immunoélectrophhérèse.
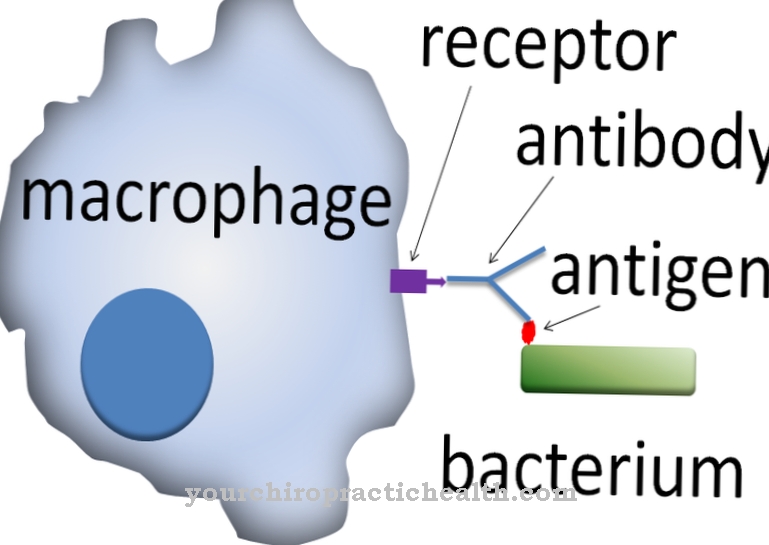
Il s'agit d'une méthode de diagnostic qualitative utilisée pour détecter les anticorps monoclonaux. Les anticorps sont des substances protéiques immunologiquement actives provenant d'une lignée cellulaire spécifique. Les anticorps monoclonaux sont tous basés sur les mêmes lymphocytes B et sont donc dirigés contre un seul épitope. Chaque réponse immunitaire naturelle aux antigènes envahissants correspond à une réponse polyclonale et est donc dirigée contre différents épitopes. Une réponse immunitaire monoclonale fournit donc des indications sur les processus corporels pathologiques.
Les anticorps monoclonaux se lient à différentes molécules avec une spécificité élevée. Cette liaison peut être démontrée au moyen d'une immunoélectrophorèse. La procédure est une procédure qualitative dans le diagnostic de laboratoire et comprend les deux types de procédure, l'électrophorèse sérique et l'immunodiffusion.
Fonction, effet et objectifs
L'immunoélectrophorèse combine la méthodologie de l'électrophorèse sérique avec l'immunodiffusion. Le sérum du patient est placé sur un gel d'agarose ou un film d'acétate de cellulose. Un sérum de contrôle est également appliqué. L'application est suivie d'une séparation électrophorétique des échantillons. Des antisérums, des IgG, des IgA, des IgM, de l'acide acétique pour l'électrophorèse normale et du kappa et du lambda sont appliqués entre les lignes de division.
Cela crée une réaction avec les anticorps dans le sérum du patient, ce qui crée des lignes de précipitation. En fonction de l'antisérum utilisé et de la position et de la forme des lignées individuelles, des conclusions peuvent être tirées sur les immunoglobulines contenues avec les chaînes légères kappa ou lambda. Dans le cas d'une bande lambda, il existe des chaînes légères libres constituées d'anticorps. Le laboratoire apporte des preuves supplémentaires via les rares IgE et IgD, ce qui permet une détermination exacte des immunoglobulines. Une méthode d'électrophorèse d'immunodiffusion a lieu selon Pierre Grabar et Curtis Williams et correspond à une combinaison d'électrophorèse sur gel d'agarose de protéines et de diffusion d'anticorps.
L'électrophorèse sur gel d'agarose a d'abord lieu. Par la suite, les anticorps contenus diffusent contre les bandes d'antigènes et créent ainsi des arcs précipités. Ceci est à distinguer de l'immunoélectrophorèse de fusée selon Laurell, qui correspond à l'électrophorèse de protéines au sein d'un gel d'agarose, dont chacune contient des anticorps à une certaine concentration. Il y a un tampon légèrement basique dans le gel, qui permet uniquement aux antigènes de migrer et qui force la plupart des anticorps au point isoélectrique par exposition à la valeur de pH légèrement basique jusqu'à ce qu'ils arrêtent de se déplacer électrophorétiquement.
Au début d'une immunoélectrophorèse de fusée, il y a un excès d'antigène, de sorte que des complexes antigène-anticorps solubles se forment. Pendant l'électrophorèse, il existe également une liaison entre les antigènes et d'autres anticorps. De cette manière, des immunoprécipités sont formés au point d'équivalence, qui ressemblent à des figures en forme de fusée avec une hauteur proportionnelle à la concentration d'antigène. La hauteur du précipité est mesurée pour évaluer le test.
Vous pouvez trouver votre médicament ici
➔ Des médicaments pour renforcer la défense et le système immunitaireRisques, effets secondaires et dangers
La détection des anticorps monoclonaux est particulièrement importante pour le diagnostic du myélome multiple et de la maladie de Waldenström. Les preuves fournies parlent d'une dégénérescence maligne des cellules immunitaires. Le myélome multiple correspond à un cancer de la moelle osseuse, qui se caractérise par la multiplication maligne des cellules productrices d'anticorps dans le plasma.
Ces plasmocytes produisent des anticorps et leurs fragments. Les plasmocytes malins proviennent toujours d'une cellule précurseur commune et sont donc génétiquement identiques. Ils ne produisent que des anticorps monoclonaux. La malignité de cette maladie peut correspondre à un stade précancéreux, mais elle peut également atteindre un stade très malin, qui sans traitement est rapidement mortel. Les symptômes de la maladie résultent de la croissance maligne des cellules ou des anticorps et fragments d'anticorps. Les symptômes les plus courants sont les douleurs osseuses, la dissolution osseuse et les fractures spontanées.
Le taux de calcium dans le sang est souvent augmenté. De plus, les anticorps anormaux se déposent souvent dans les tissus et provoquent des troubles fonctionnels dans les organes, pouvant entraîner des symptômes tels qu'une insuffisance rénale ou une altération de la circulation sanguine. La maladie de Waldström est également une maladie tumorale maligne. Plus précisément, il s'agit d'une maladie lymphomateuse maligne qui est comptée parmi les lymphomes non hodgkiniens à cellules B à progression lente et presque asymptomatiques. Dans la plupart des cas, une production anormale d'IgM monoclonale due à l'activité des cellules de lymphome malin peut être détectée dans la maladie.
La maladie de Waldenström est extrêmement similaire au myélome multiple dans ses propriétés, mais montre généralement une évolution plus favorable. La plupart des patients atteints de la maladie de Waldenström sont largement asymptomatiques au moment du diagnostic. D'autres patients présentent des symptômes précoces, tels qu'une fatigue non spécifique ou des neuropathies périphériques, qui sont causées par le dépôt d'IgM monoclonales dans la gaine de myéline. Même de petites quantités d'IgM peuvent déclencher une polyneuropathie. Aucune polyneuropathie n'apparaît chez d'autres patients, même à des niveaux élevés. De plus, des symptômes non spécifiques tels que fièvre, perte de poids indésirable ou sueurs nocturnes peuvent survenir. La douleur osseuse est également caractéristique.
En raison de la surproduction d'IgM, le sang devient hypervisceux, de sorte que les symptômes mentionnés peuvent être associés à ceux d'un syndrome d'hyperviscosité. Dans la plupart des cas, cette tendance aux saignements se manifeste par des saignements de nez fréquents, des maux de tête, un malaise général ou une vision trouble et des troubles acoustiques. Afin de détecter des maladies malignes de ce type, l'immunoélectrophhérèse est depuis longtemps devenue une procédure diagnostique standard.






.jpg)

.jpg)