le Mycoplasme génital appartient au genre des mycoplasmes. Le mycoplasme a été isolé pour la première fois sur des bovins malades en 1898. Avec le Mycoplasma pneumoniae, une forme pathogène pour l'homme a pu être détectée pour la première fois en 1962. Mycoplasma genitalium a été découvert en 1981 et attribué au genre Mycoplasma en tant que nouvelle espèce en 1983. Le séquençage complet des gènes a été publié en 1995.
Qu'est-ce que mycoplasma genitalium?
L'espèce bactérienne Mykoplasma genitalium appartient au genre Mycoplasma et à la classe superordonnée des Mollicutes. Les espèces bactériennes de la classe des Mollicutes n'ont pas de paroi cellulaire. La désignation Mollicutes signifie peau douce ou à peau douce (Molli = doux, rebondi; Cutis = peau) et l'indique.
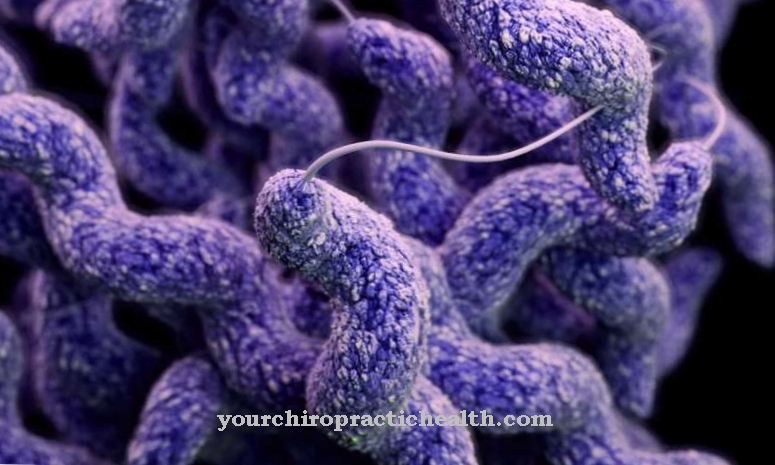
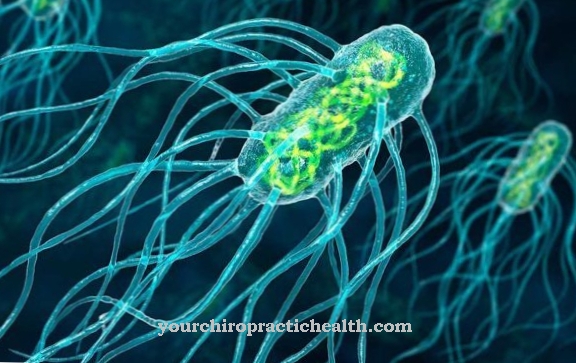
La paroi cellulaire manquante des mollicutes en général et des mycoplasmes en particulier permet une forme pléomorphe, c'est-à-dire diverse. Les bactéries apparaissent à la fois vésiculaires et filiformes et peuvent changer de forme si nécessaire. La forme filiforme du mycoplasme rappelle beaucoup un champignon, qui est exprimé dans le nom de mycoplasme. Traduit, mycoplasma (Myko = champignon et plasma = forme) signifie quelque chose comme "en forme de champignon".
En plus des propriétés pléomorphes, l'absence de paroi cellulaire provoque également une sensibilité prononcée à diverses influences environnementales. Même de légères fluctuations osmotiques dans le milieu environnant peuvent tuer les germes.
D'autre part, en raison de l'absence de paroi cellulaire, les mycoplasmes montrent également une résistance naturelle aux antibiotiques qui adhèrent à la paroi cellulaire. Les antibiotiques classiques comme les pénicillines n'ont donc aucun effet.
Les mycoplasmes sont très petits et, à 200-300 nanomètres, font partie des plus petites espèces de bactéries au monde. En raison de leur petite taille, ils jouent souvent un rôle de contaminants de laboratoire. Comme la plupart des filtres stériles produits en série n'ont pas une taille de pore nominale de 220 nanomètres, une filtration efficace du mycoplasme ne peut être garantie. Le génome du mycoplasme est l'un des plus petits génomes procaryotes au monde.
Avec 580-1 380 kbp, les mycoplasmes appartiennent aux germes les plus petits génétiquement capables de s'auto-répliquer aux côtés des nanoarchaeum equitans (~ 500 kbp) et de l'endosymbionte Carsonella ruddii (environ 160 kbp). Une autre anomalie est le cholestérol, qui est contenu dans la membrane cellulaire du mycoplasme et ne peut autrement être trouvé que dans les cellules eucaryotes.
Des études d'ARN exactes montrent que le genre des Mollicutes ne peut pas être compté comme la base de l'arbre généalogique bactérien, mais a plutôt émergé par évolution dégénérative. Une descente des germes du groupe Lactobacillus et une perte subséquente de grandes parties de l'information génétique par évolution dégénérative est très probable et fait de la classe des Mollicutes des représentants des organismes avec le plus petit génome connu.
Le petit génome du mycoplasme se prête à la recherche en synthèse, il n'est donc pas surprenant que le groupe de recherche autour de Craig Venter ait synthétisé le germe Mycoplasma genitalium en 2008. La réplique s'appelle Mycoplasma genitalium JCVI-1.0 et est considérée comme la première bactérie entièrement produite par synthèse.
Occurrence, distribution et propriétés
Les mycoplasmes ont un mode de vie parasitaire et dépendent des cellules hôtes. Ils peuvent parasiter à la fois extracellulaire sur la cellule hôte et intracellulaire. Les mycoplasmes dépendent de composants métaboliques essentiels tels que les acides aminés et nucléiques de la cellule hôte.
Il est possible de réduire le génome au besoin, ce qui est bénéfique pour un mode de vie parasitaire peu exigeant. Le mycoplasme génital s'installe dans l'urètre et vit ici préférentiellement sur les cellules épithéliales.
Maladies et affections
Les mycoplasmes sont responsables de nombreuses maladies en raison de leur mode de vie parasitaire. Avec Chlamydia trachomatis, mycoplasma genitalium est l'un des agents pathogènes les plus courants de l'urétrite non gonococcique. L'urétrite non gonococcique fait référence à une inflammation de l'urètre qui n'est pas déclenchée par les gonocoques généralement responsables.
L'urétrite s'accompagne généralement de symptômes typiques tels qu'une sensation de brûlure intense lors de la miction et un écoulement muqueux-purulent. En conséquence, les femmes peuvent avoir des saignements abondants après un rapport sexuel.
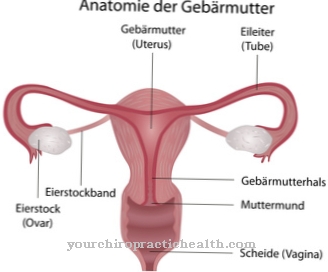
Cela peut également entraîner de graves complications chez les femmes. L'urètre beaucoup plus court peut provoquer une inflammation secondaire sévère. Des maladies inflammatoires telles que la cervicite (inflammation du col de l'utérus), l'endométrite, la salpingite et d'autres maladies inflammatoires pelviennes peuvent survenir.
Une corrélation avec d'autres plaintes et maladies telles que l'infertilité ou le cancer de l'ovaire a été statistiquement prouvée, mais n'a pas encore été prouvée de manière causale.
Une diminution du développement de la prostate a été observée chez les hommes ayant une infection antérieure et fait l'objet de discussions.
Une plus forte intensité de l'infection par le VIH par Mycoplasma genitalium est également discutée. De plus, on peut se demander si le mycoplasma genitalium doit être défini comme un pathogène sexuellement transmissible.
L'urétrite, également connue sous le nom de gonorrhée, est une maladie infectieuse communément transmise. Un traitement avec des antibiotiques est possible. Cependant, étant donné que plusieurs agents pathogènes peuvent déclencher les symptômes, l'identification de l'antigène avec toutes les résistances est essentielle pour une antibiothérapie réussie.
Pour Mycoplasma genitalium, comme pour la plupart des germes de la classe des mollicutes, un antibiotique de la classe des macrolides, en particulier l'azithromycine, est recommandé. Les macrolides n'attaquent pas le pathogène à la surface des cellules comme la pénicilline, mais empêchent la réplication ultérieure en ralentissant la synthèse des protéines du pathogène.
L'administration prématurée d'antibiotiques, en particulier de pénicilline, peut conduire à une persistance accrue de l'agent pathogène, en particulier dans le cas des germes de la classe des mollicutes.




.jpg)



.jpg)

.jpg)