Phénylalanine est un acide aminé essentiel protéinogène avec un cycle aromatique à six chaînons qui agit comme un élément constitutif de nombreuses protéines et peptides.
De plus, la phénylalanine joue un rôle important dans le métabolisme de l'azote et peut être convertie dans le foie en acide aminé protéinogène tyrosine. La phénylalanine et la tyrosine jouent un rôle important dans la synthèse de l'insuline, de la mélanine, de la thyroxine et des neurotransmetteurs dopamine, sérotonine et tyramine.
Qu'est-ce que la phénylalanine?
La phénylalanine est un acide alpha-aminé essentiel qui - contrairement à la plupart des acides aminés protéinogènes - est non seulement bioactif sous forme L, mais aussi dans une mesure limitée comme énantiomère sous forme R.
La R-phénylalanine est biochimiquement largement inactive et se produit exclusivement dans la production artificielle de l'acide aminé, mais le rôle de la D-phénylalanine dans le contrôle de certains neurotransmetteurs au sein du complexe de la douleur est en cours de discussion. En tant que caractéristique structurelle caractéristique, la phénylalanine a un cycle aromatique simple à six chaînons (cycle benzène) avec une chaîne hydrocarbonée attachée. La formule structurelle chimique est C6H5-CH2-CH (NH2) -COOH, le groupe C6H5 indiquant le cycle benzénique. L'acide aminé est amphiphile, ce qui signifie qu'il est à la fois liposoluble et hydrosoluble.
La formule chimique montre également que la phénylalanine est constituée exclusivement de carbone, d'hydrogène, d'azote et d'oxygène, des substances omniprésentes. Les métaux rares, minéraux ou oligo-éléments ne font pas partie de l'acide aminé. Cependant, le métabolisme humain ne peut pas synthétiser suffisamment la phénylalanine à partir de la tyrosine, mais dépend de l'apport alimentaire. La phénylalanine est présente en quantités suffisantes dans de nombreux aliments d'origine animale ou végétale, de sorte qu'avec une alimentation normale et mixte - en supposant une absorption normale dans le tube digestif - il n'y a pas de pénurie d'acide aminé à craindre.
Fonction, effet et tâches
La fonction et la tâche les plus importantes de la phénylalanine est de participer à la construction de nombreuses protéines et peptides. Il est également impliqué dans la synthèse de certaines hormones qui jouent un rôle central dans le contrôle des processus métaboliques.
Il existe des hormones comme l'adrénaline, la noradrénaline, la L-dopa, le PEA et la mélanine. De plus, la L-phénylalanine sert de substance basique à partir de laquelle z. B. la substance messagère dopamine, sérotonine, tyramine et autres peut être synthétisée. La L-phénylalanine sert également de matière de départ pour l'acide aminé essentiel tyrosine. A cet effet, la phénylalanine est transformée en tyrosine dans le foie en deux étapes par hydroxylation et par séparation d'une molécule d'eau. La phénylalanine hydroxylase est l'enzyme qui catalyse la conversion en tyrosine.
Un approvisionnement alternatif de la tyrosine, un acide aminé également essentiel, peut - comme avec la phénylalanine - avoir lieu par la prise alimentaire. Contrairement à tous les autres acides aminés, qui ne présentent des effets bioactifs que sous leur forme L, l'énantiomère D de la phénylalanine semble avoir au moins une influence sur la perception de la douleur. Un mélange de L- et D-phénylalanine (mélange racémique) s'est avéré avoir un effet analgésique. Le mélange DL est susceptible de bloquer la dégradation des enképhalines - les propres opioïdes du corps - de sorte que l'effet analgésique est prolongé et intensifié.
Éducation, occurrence, propriétés et valeurs optimales
L'acide aminé essentiel phénylalanine est absorbé par les aliments. Il n'est pas libre, mais fait généralement partie d'une protéine ou d'un polypeptide sous forme chimiquement liée. Afin de rendre l'acide aminé disponible pour le métabolisme, la protéine correspondante doit d'abord être décomposée au cours de la digestion, puis extraite des "fragments" en utilisant d'autres enzymes dans le métabolisme ultérieur.
La L-phénylalanine est synthétisée par la voie dite de l'acide shikimique. C'est une réaction en chaîne biocatalytique complexe que possèdent les plantes et les bactéries autotrophes. La particularité des organismes autotrophes est leur capacité à former de la matière organique à partir de matières exclusivement inorganiques. La L-phénylalanine libre a un goût amer, tandis que son énantiomère D, qui est produit exclusivement dans la production industrielle, a un goût sucré. L'acide aminé est z. B. offert comme complément alimentaire et fait également partie de l'édulcorant artificiel aspartame. La L-phénylalanine biodisponible se trouve sous forme liée dans de nombreux aliments.
Leur teneur est particulièrement élevée dans les pois secs et le soja, dans les noix et les graines de citrouille ainsi que dans divers types de poisson et de viande. Les besoins en phénylalanine dépendent fortement de l'apport de tyrosine. S'il n'y a pas de tyrosine dans l'alimentation, le corps a besoin de 38 à 52 mg par kg de masse corporelle. Avec un apport riche en tyrosine dans l'alimentation, les besoins quotidiens tombent à seulement 9 mg par kg de masse corporelle. En règle générale, les aliments contenant de la phénylalanine contiennent également une quantité correspondante de tyrosine.
La recommandation de la FAO / OMS de 1985 équivaut à un besoin combiné de L-phénylalanine et de L-tyrosine de 14 mg par kg de masse corporelle par jour. Un adulte de 80 kg de masse corporelle a donc besoin de 1 120 mg des deux substances par jour.
Maladies et troubles
Les symptômes de carence en cas d'apport permanent insuffisant de phénylalanine et de tyrosine dans l'alimentation sont extrêmement rares, mais peuvent avoir des conséquences graves, en particulier au niveau neuronal.
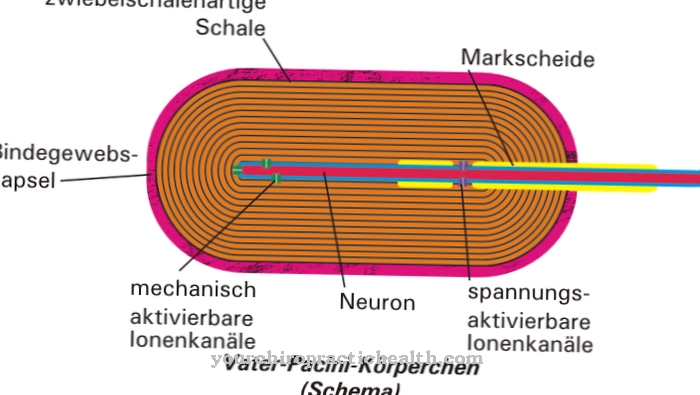
Outre une altération de la synthèse de nombreuses hormones et neurotransmetteurs, la carence peut également être indiquée par une perturbation de la myélinisation des fibres nerveuses. Le contraire d'une carence, une surconcentration de phénylalanine (phénylcétonurie), peut survenir en raison d'un trouble métabolique génétique. La maladie est héréditaire de manière autosomique récessive et conduit à une production réduite de l'enzyme phénylalanine hydroxylase, qui peut convertir la phénylalanine en tyrosine.
L'activité enzymatique réduite conduit à une forte augmentation de l'acide aminé, à ce que l'on appelle la phénylcétonurie, car la conversion en tyrosine est également la voie de dégradation de la phénylalanine. Dans le même temps, il y a un manque de tyrosine car la voie de synthèse est bloquée. Une autre maladie héréditaire dans ce contexte est le syndrome de Hartnup. C'est un trouble métabolique qui perturbe le transport de la phényalanine à travers la membrane cellulaire. Cela conduit à de graves problèmes au niveau du SNC, de la peau et du tube digestif.

.jpg)



.jpg)

.jpg)






.jpg)