Homocystéine est un acide alpha-aminé contenant du soufre non protéinogène, qui est formé comme intermédiaire à partir de la méthionine en libérant le groupe méthyle (-CH3).
Pour le traitement ultérieur de l'homocystéine, un approvisionnement adéquat en vitamines B12 et B6 ainsi qu'en acide folique ou en bétaïne en tant que fournisseur de groupes méthyle est nécessaire. Une concentration accrue d'homocystéine dans le plasma sanguin est associée à des lésions des parois des vaisseaux sanguins, à la démence et à la dépression.
Qu'est-ce que l'homocystéine?
L'homocystéine sous sa forme L bioactive est un acide aminé non protéinogène. Il ne peut pas être un élément constitutif d'une protéine car il a tendance à former un cycle hétérocyclique qui ne permet pas une liaison peptidique stable en raison de son groupe CH2 supplémentaire par rapport à la cystéine.
L'incorporation d'homocystéine dans une protéine entraînerait donc une dégradation rapide de la protéine. La formule chimique C4H9NO2S montre que l'acide aminé se compose exclusivement de substances disponibles en abondance presque partout. Les oligo-éléments, les minéraux rares et les métaux ne sont pas nécessaires à leur structure. L'homocystéine est un zwitterion car elle a deux groupes fonctionnels, chacun avec une charge positive et une charge négative, qui sont globalement électriquement équilibrés.
À température ambiante, l'homocystéine est un solide cristallin avec un point de fusion d'environ 230 à 232 degrés Celsius. Le corps peut décomposer une augmentation du taux d'homocystéine dans le sang en formant un pont disulfure entre deux molécules d'homocystéine pour former de l'homocystine et les excréter sous cette forme via les reins.
Fonction, effet et tâches
La tâche et la fonction les plus importantes de la L-homocystéine est de soutenir la synthèse des protéines et d'être convertie en S-adénosylméthionine (SAM) en coopération avec certaines co-enzymes. Avec trois groupes méthyle (-CH3), SAM est le donneur de groupe méthyle le plus important dans le métabolisme cellulaire.
La SAM est impliquée dans de nombreuses réactions de biosynthèse et de détoxification. Les groupes méthyle de certains neurotransmetteurs comme l'adrénaline, la choline et la créatine proviennent de la SAM. Après la libération d'un groupe méthyle, SAM est convertie en S-adénosylméthionine (SAH), qui est reconvertie en adénosine ou en L-homocystéine par hydrolyse. Aussi importante que soit la fonction de soutien de l'homocystéine pour certains processus métaboliques, il est également important que l'homocystéine, en tant que produit intermédiaire de ces chaînes de réaction et de synthèse biochimiques, ne se produise pas à des concentrations anormales dans le sang car elle développe alors des effets nocifs.
L'excès d'homocystéine, qui n'est pas nécessaire pour soutenir les réactions décrites ci-dessus dans le métabolisme de la méthionine, est donc normalement encore dégradé avec la participation de la vitamine B6 (pyridoxine) et excrété par les reins après la formation d'homocystine. Pour que l'homocystéine puisse remplir ses tâches métaboliques, il est important de fournir à l'organisme des quantités suffisantes de vitamines B6, B12 et d'acide folique.
Éducation, occurrence, propriétés et valeurs optimales
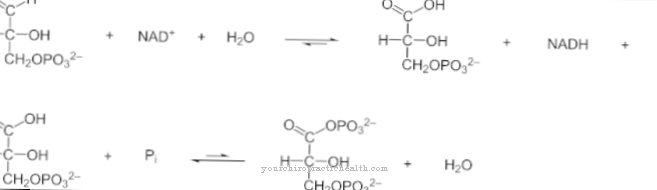
L'homocystéine est produite dans le corps en tant que produit intermédiaire de courte durée dans le métabolisme complexe de la méthionine. La désignation alternative acide (S) -2-amino-4-mercaptobutanoïque indique la structure de l'homocystéine. Il s'agit donc d'un acide monocarboxylique à groupement carboxy caractéristique (-COOH) et en même temps d'un acide gras simple. L'homocystéine n'est pas absorbée par les aliments, mais seulement temporairement produite dans le corps.
Bien que la L-cystéine bioactive joue un rôle important dans la synthèse des protéines et dans la formation de SAM, la concentration optimale et en même temps tolérable dans le sang se situe dans des limites étroites de seulement 5 à 10 µmol / litre. Des taux d'homocystéine plus élevés indiquent certains troubles métaboliques et conduisent au tableau clinique de l'hyperhomocystéinémie. Une concentration optimale de l'acide aminé dépendra probablement de l'activité mentale et physique respective et est difficile à définir. La définition d'une limite supérieure tolérable pour le taux d'homocystéine, qui devrait être d'environ 10 µmol / litre, paraît plus judicieuse.
Maladies et troubles
Si la concentration d'homocystéine dépasse la limite tolérable, il existe principalement des troubles métaboliques acquis ou déterminés génétiquement dans l'équilibre méthionine.
Souvent, il n'y a qu'un manque des vitamines B6 (pyridoxine), B9 (acide folique) et B12 (cobalamine) nécessaires, qui sont nécessaires comme coenzymes ou catalyseurs dans la chaîne de conversion biochimique. On connaît au total environ 230 mutations génétiques, quoique rares, entraînant une perturbation du métabolisme de la méthionine. L'augmentation pathologique de l'homocystéine est appelée homocystinurie. La mutation génétique la plus courante à l'origine de la maladie se situe sur le locus 21q22.3 du gène. La mutation est autosomique récessive et provoque la formation d'une enzyme défectueuse nécessaire au processus de dégradation et de conversion de l'homocystéine.
Les mutations précédemment connues sont l'omission (délétion) ou l'ajout (insertion) de nucléobases sur les brins d'ADN correspondants. Des conditions de vie et des habitudes de vie défavorables peuvent également entraîner une augmentation des taux d'homocystéine. Ceux-ci incluent la consommation excessive d'alcool, l'abus de nicotine, le surpoids et le mode de vie sédentaire. Un taux d'homocystéine excessif peut endommager l'endothélium, la paroi interne des vaisseaux sanguins et B. Promouvoir l'artériosclérose. Les veines deviennent inélastiques et provoquent un certain nombre de maladies secondaires telles que l'hypertension artérielle. Ils présentent également le risque de former des thrombus, qui provoquent des maladies coronariennes et des accidents vasculaires cérébraux.
Les maladies neurologiques telles que la dépression et la démence sénile sont également associées à une augmentation du taux d'homocystéine. Les symptômes de la maladie sont très différents chez les enfants qui souffrent d'homocystinurie génétique. Le spectre des symptômes va des caractéristiques de la maladie à peine détectables à l'apparition de presque tous les symptômes possibles. Les premiers symptômes n'apparaissent généralement qu'après avoir atteint l'âge de deux ans. Tout au plus, un ralentissement du développement psychomoteur peut être observé au cours des deux premières années de vie. Dans de nombreux cas, le premier symptôme de l'homocystinurie génétique est un prolapsus du cristallin.









.jpg)

.jpg)